近日,来自麦吉尔大学的Michael J. Meaney团队在《分子精神病学》上发表重要研究[3],首次通过全基因组关联研究(GWAS)确定了与抑郁症相关的性别特异分子通路,揭示了抑郁症的性别特异性遗传途径。
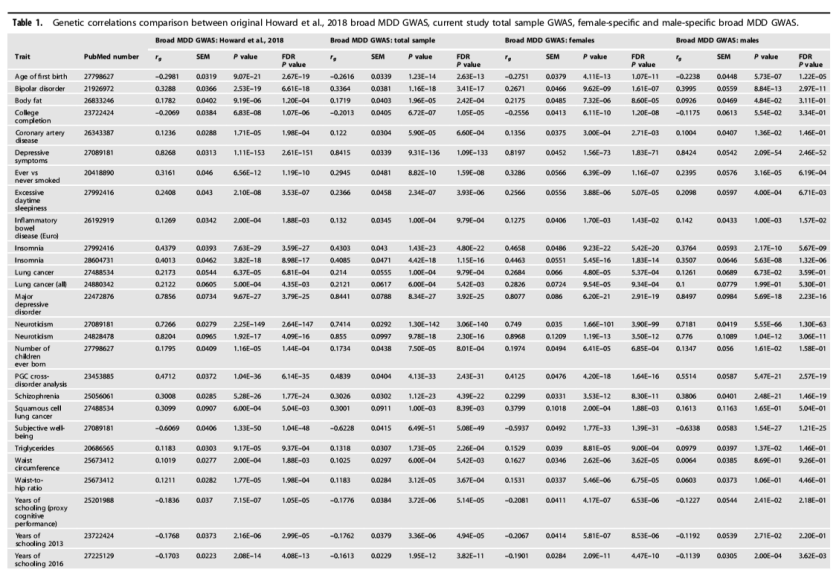
研究人员通过对英国生物库数据进行性别特异性抑郁症GWAS分析,发现女性中有11个基因位点,而男性中仅有1个基因位点与抑郁表型显著相关。同时,性别差异还影响了抑郁表型与其他临床表型的遗传相关性,如一些代谢特征(如体脂、腰围、腰臀比和甘油三酯)与抑郁表型的遗传相关性仅在女性中达到显著性水平。
此外,研究结果还表明参与抑郁症遗传和抗抑郁药靶向的生物过程在男性和女性中存在差异,这意味着治疗方法可能同样需要根据性别进行区分。这些发现进一步加深了研究人员对抑郁症性别相关遗传途径的理解。

在总人群广义性抑郁GWAS分析中,共有18个基因位点、2819个基因变异与广义性抑郁显著相关。这些结果均与先前报道的混合人群广义性抑郁GWAS分析结果相一致[4]。
紧接着,研究人员按性别将总样本分层,并分别进行GWAS分析。结果显示,在女性特异性GWAS分析中,共发现了11个基因位点与广义性抑郁显著相关,而男性中仅有1个基因位点达到显著性水平。
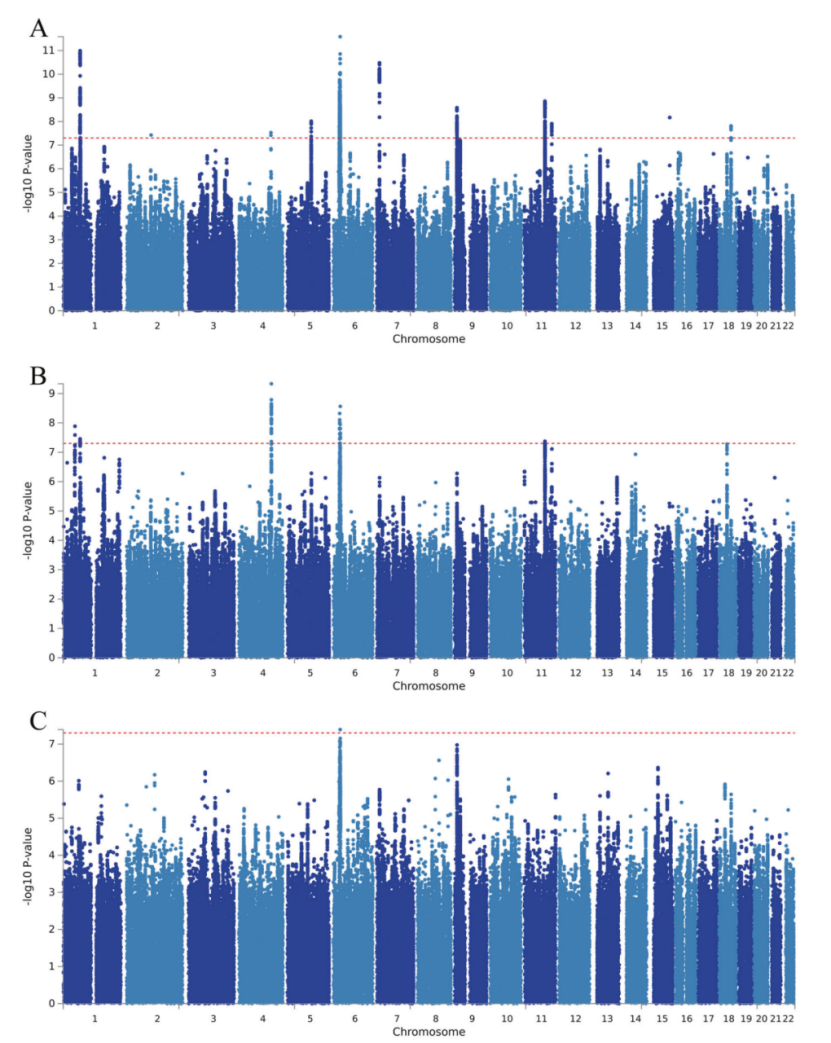
男性和女性特异性广义性抑郁GWAS相关基因富集通路存在一定交叉,其中最重要的是谷胱甘肽代谢相关通路。谷胱甘肽参与抗氧化防御,且与基因表达调节、细胞增殖、细胞凋亡、信号转导和免疫反应关系密切[6]。此外,其他交叉通路包括病毒生命周期负调控、调控病毒从宿主细胞释放、调控DNA模板转录、调控核酸模板转录、调控RNA生物合成过程以及神经认知和神经退行性疾病相关通路。
值得注意的是,“基因表达调节”是男性和女性特异性广义性抑郁GWAS相关基因富集中最常出现的基因本体论(GO)过程。然而,在男性中,“基因表达调节”映射到包括TCF4基因(一种已知的表观遗传状态调节因子,如调节DNA甲基化[7])以及大量编码组蛋白变体的基因。在女性中,“基因表达调节”则映射到与许多神经毒素相关基因、DRD2和GRM5基因。
多个精神病理学和神经退行性疾病条目与男性和女性特异性广义性抑郁GWAS基因相关,其中,参与表观遗传过程和神经递质释放调节的基因来自男性GWAS分析,而与DRD2信号相关和大量与适应性免疫相关的基因则源于女性GWAS分析。
从以上结果可以看出,男性和女性中的广义性抑郁相关基因对大脑的影响是通过独特的性别特异性机制导致的。
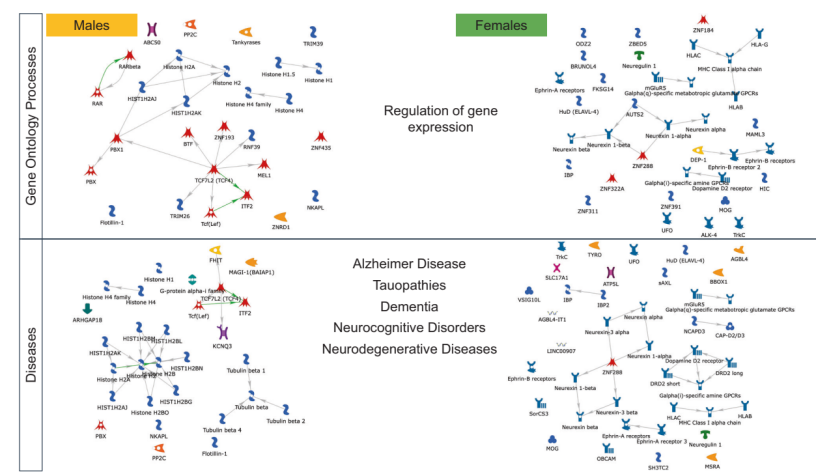
男性特异性广泛性抑郁GWAS中鉴定到的转录因子与组织和神经元分化以及表观遗传过程相关(如E2F1、Esrrb、NRSF、ZFX、ZNF423),这强调染色质重塑因子在男性发病中的潜在作用。女性特异性广泛性抑郁GWAS中鉴定到的转录因子则与氧化应激、细胞凋亡、2型糖尿病相关(如HNF3-beta、MafA、p63、RelA、VDR),这与女性中抑郁表型和代谢疾病相关表型的遗传相关性一致。
同时,研究人员还发现,与广泛性抑郁相关并可被抗抑郁药靶向的主要生物过程在男性中主要为表观遗传过程,例如染色质组装、细胞周期调节以及炎症(主要通过IL-7),在女性中则为神经元迁移、神经营养因子、突触可塑性调节以及多巴胺神经传递。
这些发现表明,参与抑郁症遗传和抗抑郁药针对的生物过程在男性和女性中存在差异,这意味着治疗方法可能同样需要根据性别进行区分。
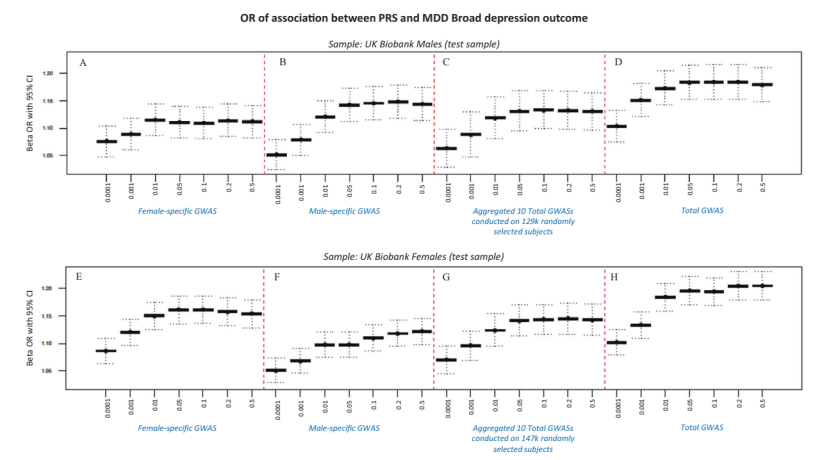
最后,研究人员通过混合、男性和女性特定GWAS计算了多基因风险评分(PRS)用以预测人群抑郁表型。结果不出所料,男性特异性PRS对男性抑郁表型结果的预测表现出比混合和女性特异性PRS更好的效果。类似地,女性特异性PRS对女性抑郁表型的预测价值优于混合和男性特异性PRS。
参考文献
1. Marcus SM, Young EA, Kerber KB, Kornstein S, Farabaugh AH, Mitchell J, Wisniewski SR, Balasubramani GK, Trivedi MH, Rush AJ: Gender differences in depression: findings from the STAR*D study. J Affect Disord 2005, 87(2-3):141-150.
2. Mackenzie CS, Reynolds K, Cairney J, Streiner DL, Sareen J: Disorder-specific mental health service use for mood and anxiety disorders: associations with age, sex, and psychiatric comorbidity. Depress Anxiety 2012, 29(3):234-242.
3. Silveira PP, Pokhvisneva I, Howard DM, Meaney MJ: A sex-specific genome-wide association study of depression phenotypes in UK Biobank. Mol Psychiatry 2023.
4. Howard DM, Adams MJ, Shirali M, Clarke TK, Marioni RE, Davies G, Coleman JRI, Alloza C, Shen X, Barbu MC et al: Genome-wide association study of depression phenotypes in UK Biobank identifies variants in excitatory synaptic pathways. Nat Commun 2018, 9(1):1470.
5. Policicchio S, Washer S, Viana J, Iatrou A, Burrage J, Hannon E, Turecki G, Kaminsky Z, Mill J, Dempster EL et al: Genome-wide DNA methylation meta-analysis in the brains of suicide completers. Transl Psychiatry 2020, 10(1):69.
6. Wu G, Fang YZ, Yang S, Lupton JR, Turner ND: Glutathione metabolism and its implications for health. J Nutr 2004, 134(3):489-492.
7. Kennedy AJ, Rahn EJ, Paulukaitis BS, Savell KE, Kordasiewicz HB, Wang J, Lewis JW, Posey J, Strange SK, Guzman-Karlsson MC et al: Tcf4 Regulates Synaptic Plasticity, DNA Methylation, and Memory Function. Cell Rep 2016, 16(10):2666-2685.
来自:
更多阅读:

